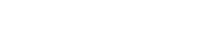Energie aus Wasser - Wie man auf dem Mond Sauerstoff und Wasserstoff produziert
In dieser Reihe von drei Aktivitäten lernen die SchülerInnen etwas über Elektrochemie.
In der ersten Aktivität werden sie einen Voltastapel bauen - eine einfache Batterie. Diese Erfindung war der Beginn der Elektrochemie.
Anschließend werden die Schüler die Elektrolyse untersuchen. Bei der Elektrolyse wird elektrischer Strom verwendet, um Wasser in seine Bestandteile aufzuspalten: Wasserstoff und Sauerstoff. Diese Produkte können als Treibstoff für Raumfahrzeuge und/oder zur Versorgung der Besatzung mit Sauerstoff verwendet werden.
In der letzten Aktivität untersuchen und benutzen die Schüler eine Brennstoffzelle.
Lernziele
Altersspanne:
14 - 16 Jahre alt
Zeit
Vorbereitung: 1 Stunde
Lektion: 2 Stunden
Lektion: 2 Stunden
Ressource verfügbar in:
Aktion 1: Baue deine eigene Batterie
Bei dieser Aktivität bauen die SchülerInnen einen Voltastapel - eine einfache Batterie - aus Metallplatten, Geschirrtüchern und Essig. Ein Voltahaufen nutzt eine spontane chemische Reaktion, um Elektrizität zu erzeugen.

Ausrüstung
Aktion 2: Elektrolyse
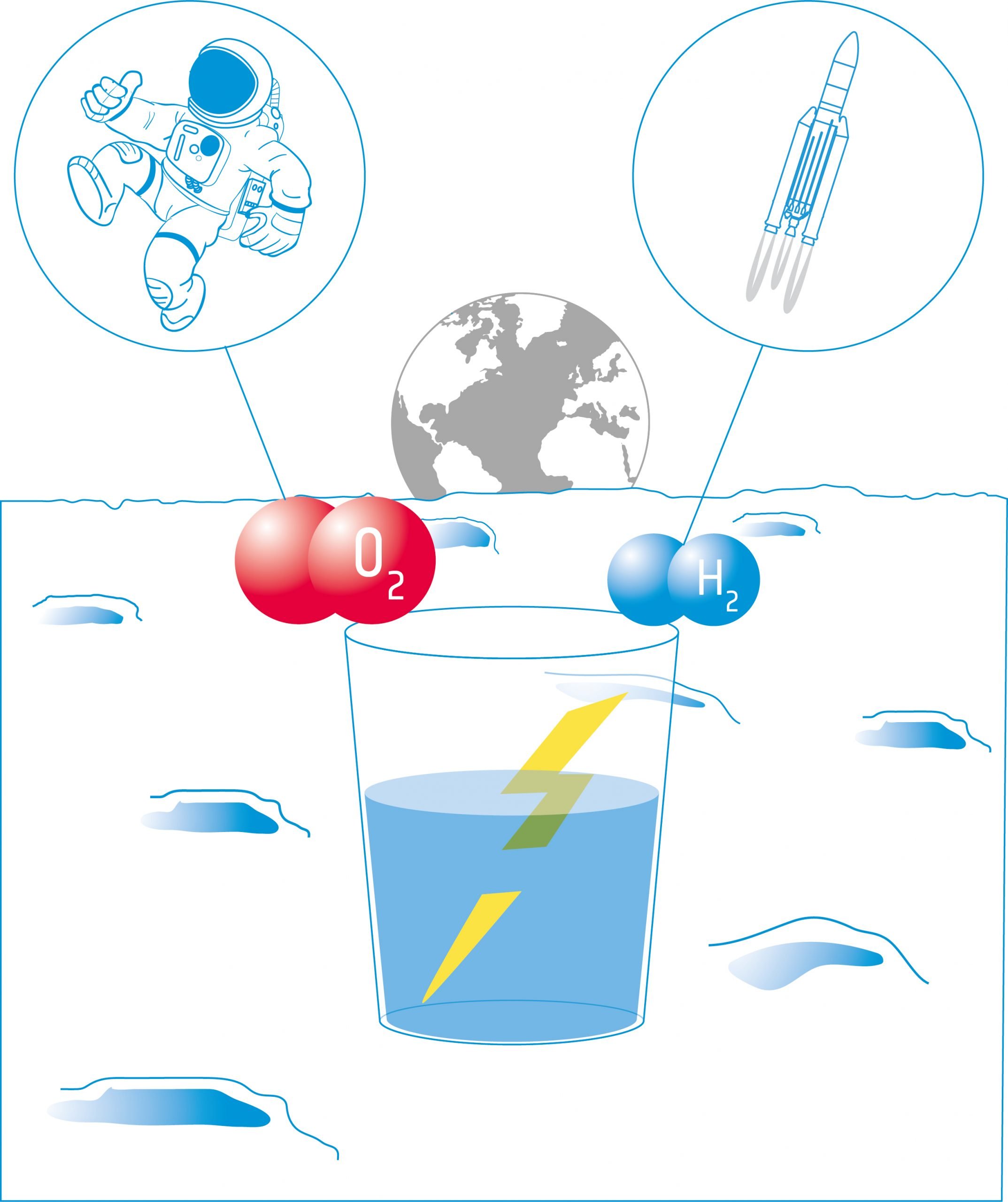
In dieser Aktivität bauen die Schüler einen Elektrolyseur: ein Gerät, das mithilfe von zwei Elektroden elektrischen Strom in eine Flüssigkeit einleitet. Sie verwenden das Gerät für die Wasserelektrolyse und entdecken, dass es möglich ist, Wasser in seine Bestandteile aufzuspalten: Sauerstoff und Wasserstoff.
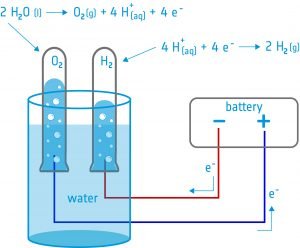
Ausrüstung
Aktion 3: Brennstoffzelle
In dieser Aktivität werden die Schüler die Produkte der Wasserelektrolyse (H2 und O2) in einer Brennstoffzelle. Sie untersuchen, wie Brennstoffzellen durch eine chemische Reaktion Strom und Wärme erzeugen. Die SchülerInnen betrachten die Möglichkeiten und Grenzen von Brennstoffzellen für die Erforschung des Mondes.
Ausrüstung
Wussten Sie das?
Die Elektrolyse von Wasser ist die wichtigste Methode zur Erzeugung von Sauerstoff an Bord der Internationalen Raumstation (ISS). Das Wasser wird aus Urin, Abwasser und Kondenswasser gesammelt und im Oxygen Generation System (OGS) in Sauerstoff und Wasserstoff gespalten.
Die fußballfeldgroßen Solarzellen der Station sind die Energiequelle. Ein ähnliches System könnte auch auf dem Mond eingesetzt werden.
Die fußballfeldgroßen Solarzellen der Station sind die Energiequelle. Ein ähnliches System könnte auch auf dem Mond eingesetzt werden.

Die ISS in der Erdumlaufbahn
Schlüsselwörter:

Moon Shelter - Erforschung verschiedener Schutzräume auf der Erde und im Weltraum
Kurzbeschreibung: In dieser Reihe von Aktivitäten analysieren die Schülerinnen und Schüler die Bedeutung von Unterkünften zum Schutz auf der Erde und im Weltraum. Die SchülerInnen vergleichen
AstroCrops - Pflanzenzucht für künftige Weltraummissionen
Kurzbeschreibung: In dieser Reihe von Aktivitäten werden die Schüler ein Verständnis für Keimung und Pflanzenwachstum entwickeln, indem sie die Entwicklung von drei unbekannten Pflanzen verfolgen
Kann Leben in fremden Umgebungen überleben? - Definition von für Leben geeigneten Umgebungen
Kurzbeschreibung: In dieser Aktivität überlegen die Schüler, ob Leben, das in extremen Umgebungen auf der Erde gefunden wurde, auch anderswo im Sonnensystem überleben könnte. Die SchülerInnen werden