Kraft fra vann – Hvordan produsere oksygen og hydrogen på månen
I dette settet med tre aktiviteter vil elevene lære om elektrokjemi.
I den første aktiviteten skal de bygge en voltaisk haug - et enkelt batteri. Denne oppfinnelsen markerte begynnelsen på elektrokjemien.
Elevene skal deretter studere elektrolyse. Elektrolyse bruker elektrisk strøm til å spalte vann i sine bestanddeler: hydrogen og oksygen. Disse produktene kan brukes som drivstoff for romfartøy og/eller for å gi oksygen til mannskapet.
I den siste aktiviteten undersøker og bruker elevene en brenselcelle.
Læringsmål
Aldersgruppe:
14 - 16 år gammel
Tid
Forberedelse: 1 time
Leksjon: 2 timer
Leksjon: 2 timer
Ressurs tilgjengelig i:
Aktivitet 1: Bygg ditt eget batteri
I denne aktiviteten skal elevene konstruere en voltaisk haug - et enkelt batteri - av metallplater, oppvaskklut og eddik. En voltaisk haug bruker en spontan kjemisk reaksjon for å skape elektrisitet.

Utstyr
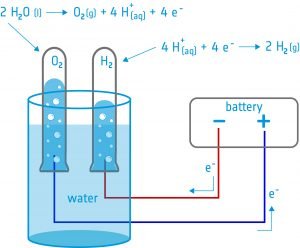
Aktivitet 2: Elektrolyse
I denne aktiviteten skal elevene bygge en elektrolysator: et apparat som fører elektrisk strøm inn i en væske ved hjelp av to elektroder. De skal bruke apparatet til vannelektrolyse og oppdage at det er mulig å spalte vann i dets bestanddeler: oksygen og hydrogen.
Utstyr
Aktivitet 3: Brenselcelle
I denne aktiviteten skal elevene bruke produktene fra vannelektrolyse (H2 og O2) i en brenselcelle. De skal undersøke hvordan brenselceller produserer elektrisitet og varme fra en kjemisk reaksjon. Elevene skal vurdere mulighetene og begrensningene ved brenselceller for utforskning av månen.
Utstyr
Visste du det?
Elektrolyse av vann er den viktigste metoden for å generere oksygen om bord på Den internasjonale romstasjonen (ISS). Vann samles inn fra urin, avløpsvann og kondensvann og spaltes i oksygen og hydrogen i Oxygen Generation System (OGS).
Stasjonens solcellepaneler på størrelse med en fotballbane er strømkilden. Et lignende system kan brukes på månen.
Stasjonens solcellepaneler på størrelse med en fotballbane er strømkilden. Et lignende system kan brukes på månen.

ISS i bane rundt jorden

Vann på månen – Filtrering av månens iskjerner for å trekke ut vann
Kort beskrivelse: I denne ressursen skal elevene bruke en dag på å registrere omtrent hvor mye vann de bruker til ulike aktiviteter. Dette etterfølges av en

Moon Rover – Bygger en solcelledrevet rover
Kort beskrivelse: I denne aktiviteten skal elevene sammenligne fordeler og ulemper ved fornybare energikilder og ikke-fornybare energikilder og studere enkle elektriske kretsløp.

Kjennetegn på et stjerneskudd - Kometer, meteorer og kratere i solsystemet
Kort beskrivelse: I mange gamle sivilisasjoner var fortellingen om et stjerneskudd et varsel om ting som skulle komme. I denne aktivitetsserien får elevene